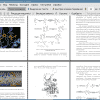
Тема: Синтез и противоопухолевая активность производных 2-аминопиримидина
Характеристики работы
Закажите новую по вашим требованиям
Представленный материал является образцом учебного исследования, примером структуры и содержания учебного исследования по заявленной теме. Размещён исключительно в информационных и ознакомительных целях.
Workspay.ru оказывает информационные услуги по сбору, обработке и структурированию материалов в соответствии с требованиями заказчика.
Размещение материала не означает публикацию произведения впервые и не предполагает передачу исключительных авторских прав третьим лицам.
Материал не предназначен для дословной сдачи в образовательные организации и требует самостоятельной переработки с соблюдением законодательства Российской Федерации об авторском праве и принципов академической добросовестности.
Авторские права на исходные материалы принадлежат их законным правообладателям. В случае возникновения вопросов, связанных с размещённым материалом, просим направить обращение через форму обратной связи.
📋 Содержание
ВВЕДЕНИЕ 7
1 Цитотоксичность 8
2 Тирозинкиназы 10
2.1 BCR-ABL тирозинкиназы 11
2.2 EGFR тирозинкиназы 12
3 Синтезы ингибиторов тирозинкиназы на основе 2-аминопиримидина 14
3.1 Синтезы ингибиторов BCR-ABL 14
3.2 Синтезы ингибиторов EGFR тирозинкиназы 27
ЗАКЛЮЧЕНИЕ 44
СПИСОК ИСПОЛЬЗУЕМОЙ ЛИТЕРАТУРЫ 45
📖 Введение
Производные 2-аминопиримидина способны предотвращать активацию тирозинкиназы, что приводит к специфичному для мишени ингибированию пролиферации клеток [3]. Поиск специфических ингибиторов BCR-ABL тирозинкиназы среди 2-аминопиримидинов завершился открытием препарата Гливек в 1995 году, применяемого при лечении ХМЛ и ОЛЛ [4-6].
В последние несколько лет производные на основе 2-аминопиримидина были исследованы на ингибирующую активность EGFR-киназы. Так, Осимертиниб был одобрен FDA в 2015 году для лечения пациентов с немелкоклеточным раком легких [7].
Поскольку производные, полученные на основе 2-аминопиримидина, обладают противоопухолевыми свойствами, разработка новых методов синтеза потенциальных противоопухолевых соединений представляет большой интерес [4-6].
Целью работы является анализ литературы, в которых содержатся новые подходы по получению производных 2-аминопиримидина, обладающих антипролиферативными свойствами среди синтетических соединений, в связи с чем поставлены следующие задачи:
1) изучить природу и функции BCR-ABL и EGFR тирозинкиназ;
2) изучить литературные данные о способах получения производных 2- аминопиримидина, ингибирующие данные мишени;
3) критически обобщить проанализированную литературу.
✅ Заключение
В работе рассмотрены подходы к синтезу различных производных на основе 2-аминопиримидина, являющихся ингибиторами для указанных мишеней. Оценка цитотоксичности по отношению к клеточным линиям K562 (для BCR-ABL тирозинкиназы) и H1975, несущей EGFRL858R, eGFRL858R/T790M (для EGFR тирозинкиназы) позволила выделить наиболее эффективные ингибиторы. С помощью молекулярного докинга исследуемых соединений, проявивших высокую селективность, была оценена степень их комплементарности с активным центром мишеней.
В заключение можно сказать, что среди описанных вновь синтезированных соединений есть те, которые проявляют антипролиферативную активность наравне или выше уже существующих препаратов, что говорит об их перспективности и возможности использования в дальнейших клинических испытаниях.