Тема: Синтез селективного ингибитора протеинкиназы ES013 и разработка принципиальной технологической схемы
Закажите новую по вашим требованиям
Представленный материал является образцом учебного исследования, примером структуры и содержания учебного исследования по заявленной теме. Размещён исключительно в информационных и ознакомительных целях.
Workspay.ru оказывает информационные услуги по сбору, обработке и структурированию материалов в соответствии с требованиями заказчика.
Размещение материала не означает публикацию произведения впервые и не предполагает передачу исключительных авторских прав третьим лицам.
Материал не предназначен для дословной сдачи в образовательные организации и требует самостоятельной переработки с соблюдением законодательства Российской Федерации об авторском праве и принципов академической добросовестности.
Авторские права на исходные материалы принадлежат их законным правообладателям. В случае возникновения вопросов, связанных с размещённым материалом, просим направить обращение через форму обратной связи.
📋 Содержание
ВВЕДЕНИЕ
1.ЛИТЕРАТУРНЫЙ ОБЗОР
1.1.Перспективы использования производных имидазо[2,1 -й]тиазола в
медицине
1.2.Способы получения производных имидазо[2,1-^]тиазола
1.3.Химические свойства имидазо[2,1-^]тиазолов
1.4.Особенности технологии производства действующих компонентов
лекарственных препаратов
2.ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
2.1.Разработка синтетического подхода к получению ингибитора ES013
2.2.Биологические испытания ингибитора ES013
2.3.Материальный баланс производства
2.4.Разработка принципиальной технологической схемы производства
ингибитора ES013
3.ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
3.1.Реагенты, вспомогательные материалы и оборудование
3.2.Подготовка растворителей
3.3.Синтез исходных и целевых соединений
ЗАКЛЮЧЕНИЕ
СПИСОК ЛИТЕРАТУРЫ
ПРИЛОЖЕНИЕ
📖 Введение
технологической схемы производства низкомолекулярного ингибитора EGFR-киназы на основе гетеросистемы имидазо[2,1-^]тиазола.
Для реализации цели были поставлены следующие задачи:
Во-первых, посредствам компьютерного моделирования
оптимизировать структуру гетеросистемы имидазо[2,1-^]тиазола с учетом наибольшей вероятности проявления ингибирующих свойств.
Во-вторых, разработать синтетический подход к получению производных имидазо[2,1-^]тиазола заданной структуры.
В-третьих, осуществить доказательство структуры синтезированного производного имидазо[2,1 -й]тиазола.
В-четвертых, исследовать ингибирующие свойства производного имидазо [2,1 -й]тиазола.
В-пятых, разработать принципиальную технологическую схему производства низкомолекулярного ингибитора EGFR-киназы ES013.
Развитие медицинской химии неразрывно связано с поиском и разработкой новых, более действенных и безопасных препаратов. При растущей необходимости ускорения темпов разработки новых лекарств, путь от химического соединения до лекарственного средства является довольно долгим. Однако сократить финансовые затраты и время поиска соединений, обладающих требуемыми свойствами, позволяет компьютерное моделирование. Представленная магистерская работа посвящена разработке нового селективного низкомолекулярного ингибитора протеинкиназы на основе имидазо[2,1-^]тиазола с применением современных методов компьютерного моделирования.
Протеинкиназы относятся к довольно большой группе регуляторных белков, отвечающих за многие процессы в клетке, в том числе и за патологические процессы онкогенеза. Данные исследования направлены на создание веществ с заранее заданными биологическими свойствами. Решение поставленной задачи складывается из следующих логических этапов: молекулярное моделирование - синтез - доказательство структуры - биологические испытания - разработка принципиальной технологической схемы.
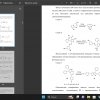
Гетеросистема имидазо[2,1-^]тиазола была использована в качестве основы низкомолекулярного ингибитора, поскольку ее производные являются составной частью некоторых весьма значимых биологически активных молекул и лекарственных веществ. Например, 6- фенилимидазотиазол входит в состав коммерчески доступных препаратов Тетрамизола и Левамизола, обладающих иммуномодулирующим, а также противоглистным действием. В последние годы интерес к данной гетеросистеме продолжает увеличиваться, в пользу чего свидетельствует растущее количество публикаций, описывающих синтез новых производных имидазо[2,1-^]тиазола и результаты исследований их фармакологической активности. Среди всего разнообразия видов биологической активности данного класса соединений особенно отметим противораковую, антиокислительную, антиаллергическую, противомикробную активности и ряд других свойств. С другой стороны, используемые в настоящее время ингибиторы протеинкиназ, имеют в качестве базовой части в большинстве случаев гетеросистемы пиримидина и хиназолина, в связи с этим разработка ингибитора на основе гетеросистемы имидазо[2,1-^]тиазола является новым и актуальным направлением.
Резюмируя вышесказанное можно сделать вывод, что тема работы является актуальной, а полученные в процессе ее развития соединения - перспективными, как вещества с заданными биологическими свойствами.
✅ Заключение
2.Получен ряд новых производных имидазо[2,1-^]тиазола, строение которых подтверждено методами ядерного магнитного резонанса и рентгеноструктурного анализа.
3.При помощи молекулярного моделирования определено соединение -
лидер, которое с большой вероятностью может оказаться эффективным противораковым агентом - 5-(2-(4-(нафтален-1-ил)пиперазин-1-
ил)тиазол-5-ил)-6- фенилимидазо [2,1 -й]тиазол.
4.Проведена модификация первоначальной синтетической схемы, позволившая сократить число стадий и отказаться от использования таких агрессивных реагентов, как молекулярный бром и соляная кислота.
5.Проведен полный синтез 5-(2-(4-(нафтален-1-ил)пиперазин-1-
ил)тиазол-5-ил)-6-фенилимидазо[2,1-^]тиазола и оценена его
противораковая активность. Показано, что данное производное обладает противораковыми свойствами в микромолярных концентрациях.
6.Разработана принципиальная технологическая схема получения 5-(2-(4- (нафтален-1 -ил)пиперазин-1 -ил)тиазол-5-ил)-6-фенилимидазо[2,1 - й]тиазола, которая может быть применима для широкого круга производных данной гетеросистемы.
7.Результаты работы апробированы на XX Менделеевском съезде по общей и прикладной химии и на ХХ Всероссийской конференции молодых ученых-химиков (с международным участием).