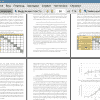
Тема: Генетическое разнообразие и инфекционные свойства микроспоридий чешуекрылых насекомых
Характеристики работы
Закажите новую по вашим требованиям
Представленный материал является образцом учебного исследования, примером структуры и содержания учебного исследования по заявленной теме. Размещён исключительно в информационных и ознакомительных целях.
Workspay.ru оказывает информационные услуги по сбору, обработке и структурированию материалов в соответствии с требованиями заказчика.
Размещение материала не означает публикацию произведения впервые и не предполагает передачу исключительных авторских прав третьим лицам.
Материал не предназначен для дословной сдачи в образовательные организации и требует самостоятельной переработки с соблюдением законодательства Российской Федерации об авторском праве и принципов академической добросовестности.
Авторские права на исходные материалы принадлежат их законным правообладателям. В случае возникновения вопросов, связанных с размещённым материалом, просим направить обращение через форму обратной связи.
📋 Содержание
Глава 1. Литературный обзор по теме исследования 7
1.1. Общая характеристика микроспоридий 7
1.1.1. Общее строение микроспоридий 7
1.1.2. Жизненный цикл микроспоридий 11
1.1.3. Циклы развития микроспоридий 13
1.1.4 Пути передачи микроспоридий 14
1.1.5 Тканевая локализация и специфичность микроспоридий 16
1.2. Защитные реакции насекомых 18
1.3. Геном микроспоридий 19
1.4. Филогенетическое положение микроспоридий 20
1.5. Практическое значение микроспоридий 23
Глава 2. Материалы и методы исследования 27
2.1. Материалы исследования 27
2.1.1. Объект исследования 27
2.2. Методы исследования, используемые в работе 27
2.2.1. Содержание насекомых в лабораторных условиях 27
2.2.2. Экстракция ДНК с помощью СТАБ 29
2.2.3. Полимеразная цепная реакция (ПЦР) 30
2.2.4. Электрофорез в агарозном геле 31
2.2.5. Выделение и очистка ДНК из агарозного геля (Gene Clean) и определение количества ДНК в пробе 32
Глава 3. Результаты и обсуждение 34
3.1. Изучение видового состава и распространённости микроспоридий в популяциях массовых видов чешуекрылых-фитофагов 34
3.1.1. Молекулярно-филогенетический анализ микроспоридий, выделенных из представителей сем. Noctuidae 34
3.1.2. Филогенетическая реконструкция микроспоридий, выделенных из представителей сборной группы дендрофаги 40
3.1.3. Молекулярно-филогенетический анализ микроспоридий, выделенных из представителей сем. Pieridae 47
3.2. Изучение инфекционных свойств микроспоридий р. Nosema 52
3.2.1. Инфекционные свойства Nosema bombycis 53
3.2.2. Инфекционные свойства Nosema pyrausta 57
3.2.3. Инфекционные свойства Nosema tyriae 59
3.2.4. Инфекционные свойства Nosema polyvora 63
3.3. Изучение взаимоотношения микроспоридий чешуекрылых с энтомофагами 69
Заключение 74
Выводы 78
Благодарности 79
Список литературы 80
Приложение 91
Приложение 1 91
Приложение 2 96
Приложение 3 103
Приложение 4 108
Приложение 5 113
📖 Введение
В России изучением микроспоридий занимаются на протяжение более 70 лет, и в настоящее время сложились предпосылки для углублённого анализа паразито-хозяинных отношений с использованием современных методов молекулярно-биологического анализа (Issi, 2020). Энтомопатогены, собранные во вторую половину XX века не были изучены молекулярно-генетическими методами, что позволит дополнить и углубить знания, полученные ранее. В настоящее время филогенетический анализ SSU на основе рРНК микроспоридий стал обязательной частью для описания вида. Сопоставление уже имеющихся данных по биологическим свойствам патогенов с новыми (на основе молекулярно-генетического анализа) позволит углубить знания, полученные ранее (Sokolova et al., 2018).
Особый интерес представляют собой патогенные микроспоридии для ряда вредных чешуекрылых насекомых с точки зрения дальнейших перспектив их использования в борьбе с вредителями (Grushevaya et al., 2021; Issi & Tkach, 1971; Issi, 2020). Большинство микроспоридий вызывают медленное отмирание насекомых, что позволяет им оставаться длительное время в популяции хозяина на достаточном уровне, вызывая снижение жизнеспособности: уменьшается плодовитость, продолжительность жизни насекомых, повышается чувствительность к неблагоприятным факторам (Goblirsch, 2018; Le Brun et al., 2022). Кроме того, микроспоридии передаются также и новому поколению трансовариальным и псевдотрансовариальным путями, что делает их перспективными на длительный период времени в борьбе с вредителями (Goertz & Hoch, 2008; Kashkarova & Khakhanov, 1980; Le Brun et al., 2022). Среди наиболее изученных микроспоридий у 4 насекомых можно выделить три вида паразитов хозяйственно значимых насекомых - N. bombycis из тутового шелкопряда и V. apis и V. ceranae из медоносной пчёлы (Goblirsch, 2018; Pei et al., 2021).
Кроме основных хозяев, микроспоридии чешуекрылых способны заражать перепончатокрылых энтомофагов (паразитоидов). Эти взаимодействия интересны тем, что микроспоридия способна существовать в представителях сразу двух разных отрядов насекомых. Для многих энтомофагов уже изучены естественные (типичные) микроспоридии, которые встречаются в их основных хозяевах (Kermani et al., 2014; Schuld et al., 1999; Simoes et al., 2012) и способны распространяться посредством паразитоидов. Кроме того, энтомопатогены могут оказывать сильное патологическое воздействие на паразитических ос, вызывая смертность на личиночной стадии, снижение жизнеспособности и плодовитости взрослых насекомых. Понимание этих факторов важно для изучения способности наездников быть успешными распространителями микроспоридий в популяциях массовых чешуекрылых, оставаясь на достаточном уровне для регулирования численности насекомых (Kermani et al., 2014; Schuld et al., 1999).
Таким образом, цель работы состоит в изучении разнообразия микроспоридий, выделенных из представителей отряда Lepidoptera, и их способности заражать другие виды чешуекрылых-фитофагов, а также перепончатокрылых энтомофагов.
Для достижения поставленной цели необходимо выполнить следующие задачи.
1. Оценить видовой состав микроспоридий в популяциях массовых видов чешуекрылых-фитофагов;
2. Оценить способность микроспоридий различных видов к заражению модельных насекомых-хозяев при их культивировании в лабораторных условиях;
3. Изучить взаимоотношения микроспоридий чешуекрылых с энтомофагами.
Научная новизна. При выполнении работы были получены новые данные о видовом составе микроспоридий, выделенных из представителей отряда Lepidoptera (в основном из сем. Pieridae, Erebidae, Noctuidae и Bombycoidea). Было получено 26 сиквенсов мсрРНК микроспоридий для проб, хранившихся в коллекции ВИЗР на протяжение 70 лет. Их анализ впервые позволил установить филогенетическое положение ряда изолятов микроспоридий. Кроме образцов, полученных в прошлом веке, были проанализированы гусеницы и бабочки, собранные за 2017-2021 г.г., что позволило обнаружить ещё 7 изолятов микроспоридий. Была изучена инфекционность четырех близкородственных видов микроспоридий в лабораторных условиях по отношению к разным чешуекрылым хозяевам из различных семейств (Crambidae, Nymphalidae, Pieridae, Erebidae, Bombycidae, Pyralidae, Plutellidae, Sphingidae, Yponomeutidae). Кроме того, было изучено влияние микроспоридий не только на неспецифического чешуекрылого хозяина, но и на его паразитоида, что важно для совершенствования подходов к борьбе с вредными чешуекрылыми насекомыми.
✅ Заключение
Исследование новых изолятов микроспоридий, собранных в 2017-2021 гг., позволило получить 7 последовательностей, которые принадлежит к двум родам - Nosema и Vairimorpha.
С некоторыми изолятами (Nosema polyvora и Nosema sp. ex Helicoverpa zea SouthWestern Russia 2019 (данные по инфекционным свойствам последнего изолята представлены в недавно опубликованной статье - Kononchuk et al., 2022) были поставлены опыты по искусственному скармливанию спор различным представителям чешуекрылых насекомых, изучаемых в данной работе.
В современных сборах 2020-2021 гг. удалось найти насекомых, пораженных микроспоридиями, идентичных изолятам из коллекции ВИЗР, собранной в середине прошлого века. Энтомопатогены схожи по строению (форма и размер спор), генотипу (по секвенированному фрагменту гена мсрРНК) и по инфекционным свойствам (выделены из тех же хозяев). В частности, были обнаружены споры N. polyvora, которые не встречались в сборах капустной белянки с 1975 года. Помимо этой микроспоридии, был найден изолят, принадлежащий к роду Vairimorpha - V. mesnili. Первоначально эти два изолята описывались как два разных вида, но в виду своеобразного жизненного цикла Vairimorpha mesnili (с образованием октоспор) было выдвинуто предположение, что Nosema polyvora - это часть сложного цикла V. mesnili (Sprague, 1977). В дальнейшем находили только споры характерные для V. mesnili (Yaman et al., 2014). И только сравнительно недавно, нами были обнаружены оба изолята, и при помощи молекулярной диагностики было показано, что это два разных вида, которые заняли место в разных кладах на филогенетическом дереве.
В ходе проведенных нами сборов насекомых, был найден новый хозяин для N. polyvora. В частности, в пробе Nosema sp. ex Mamestra brassicae 1962, были обнаружены споры, напоминающие по форме и размерам энтомопатоген, выделенный из капустной белянки. После экстракции ДНК была получена нуклеотидная последовательность данного образца. При сравнении с N. polyvora из проб, выделенных из коллекции и из новых сборов, оказалось, что они идентичны по данному локусу на 100%. Раньше предполагали, что N. polyvora достаточно узкоспецифичная микроспоридия и воздействует только на представителей семейства Pieridae (Issi & Maslennikova, 1966), но на основе последних данных, включая поставленные опыты, можно предположить, что эта паразитарная система сложнее, чем считалось ранее. В ней задействовано по крайней мере 6 представителей из отряда Lepidoptera (Mamestra brassicae, Pieris rapae, Pieris brassicae, Pieris napi, Aporia crataegi, Plutella xylostella), как минимум один представитель из отряда Braconidae (Cotesia glomerata) и его гиперпаразитоиды из отряда Ichneumonidae (Gelis agilis и Lysibia nana) (Issi & Maslennikova, 1966; Junnikkala, 1985; Yoshinori, 1955). Вероятно, это ещё не полный список хозяев, так как паразитоидов намного больше среди всех шести видов, кроме того, на капусте могут обитать и другие вредители (другие гусеницы чешуекрылых, клопы, жуки, тля и т.д.).
Из новых сборов был отобран изолят N. polyvora, с которым было поставлено несколько биотестов. Для этой микроспоридии был известен небольшой круг хозяев, включающий представителей из р. Pieris и р. Aporia - капустная (были поставлены опыты на этом объекте), репная, брюквенная и горчичная белянки, а также боярышница (Issi & Maslennikova, 1966). Среди новых обнаруженных хозяев можно отметить капустную моль. При этом на данный момент не было сообщений о нахождение спор N. polyvora в этих гусеницах и бабочках в природе. Также стоит отметить стеблевого мотылька, но в качестве резистентной модели хозяина.
Nosema pyrausta представляет собой удобный объект, который успешно культивируется в лабораторных условиях в стеблевом и кукурузных мотыльках в течение года. Это даёт возможность не потерять инфекционные свойства микроспоридии, а также ставить опыты круглогодично с разными насекомыми. Однако этот паразит оказался более узкоспецифичным - он инфицирует в высокой степени четыре вида травяных огневок и крапивницу, тогда как остальные насекомые, которые чувствительны к данному патогену в меньшей степени (пчелиная огневка, непарный шелкопряд) могут рассматриваться как резистентные модели (Grushevaya et al., 2020, 2021; Kononchuk et al., 2021; Malysh et al., 2021; Tokarev et al., 2018).
Отдельное внимание стоит уделить N. tyriae, описанной ранее только в одной статье (Canning et al., 1999). В ходе данной работы удалось выявить способность данного вида заражать многих хозяев, таких как стеблевой мотылёк, капустница, брюквенница и капустная моль. Данный энтомопатоген был высоковирулентным для отдельных видов (например, для капустной и брюквенной белянки), но для остальных насекомых он не оказывал сильного патологического воздействия с высоким летальным исходом. Это свойство данного энтомопатогена интересно с точки зрения изучения передачи инфекции и ее влияния на следующее поколению насекомых, а также с точки зрения перспектив его использования для борьбы с вредными чешуекрылыми.
Наибольшее количество данных было найдено и получено для микроспоридии Nosema bombycis, которая имеет широкий круг хозяев. Среди ранее изученных восприимчивых насекомых можно выделить представителей сем. Noctuidae и Pieridae, которые после инфицирования не могли иметь здоровое потомство (Kashkarova & Khakhanov, 1980; Pei et al., 2021). Среди обнаруженных нами хозяев можно выделить стеблевого мотылька, крапивницу, капустную и яблонную молей. Сейчас вновь поднимаются вопросы о возможности использования N. bombycis в качестве агента для борьбы с вредными чешуекрылыми, в частности против Spodoptera litura и Helicoverpa armigera (Imura et al., 2019). Данные, полученные в ходе этой работы, позволили углубить и дополнить уже имеющиеся сведения об этом энтомопатогене, а также расширить представления о потенциальном круге его хозяев.
Микроспоридии оказывают сильное влияние на организм хозяина: возможны проявления каннибализма среди гусениц, нарушение водного баланса, изменения цвета личинок, снижение активности в целом и т.д. (Andreadis, 2007; Issi & Maslennikova, 1966; Vavra & Lukes, 2013; Исси, 1963). Почти все признаки заболевания были обнаружены в данных опытах. Кроме того, микроспоридиоз вызывает высокую смертность гусениц младших или старших возрастов (Nosema bombycis и крапивница/капустница) (Kashkarova & Khakhanov, 1980), или происходит искусственная пролонгация жизни насекомого, необходимая для созревания наибольшего количества спор (N. bombycis и яблонная моль). Эти паразиты являются для личинок сильнейшим фактором стресса, из-за которого они впоследствии не могут сформировать полноценную куколку (N. tyriae и американская белая бабочка). Изучение таких эффектов, вызываемых микроспоридиями, важно для понимания возможности использования этих энтомопатогенов не только в лабораторных условиях, но и во внешней среде против вредных насекомых.
Нетипичная микроспоридия способна инфицировать паразитоида в хозяине наравне с типичной. Так, N. bombycis способна заражать капустную белянку и паразитоида Cotesia glomerata в ней. Похожая ситуация отмечена и в двух других хорошо изученных природных паразитарных системах с участием N. polyvora и Vairimorpha mesnili (Issi & Maslennikova, 1966; Larsson, 1979; Исси и Онацкий, 1982). Причём, как и ранее было отмечено, выход апантелеса происходил примерно в одно и тоже время с контролем, количество личинок паразитоида также совпадало с незаражённым вариантом. Однако, в соответствии как с литературными, так и с нашими данными, отличалось количество личинок, которые не смогли сплести кокон в инфицированных вариантах (доля личинок апантелеса, которые смогли сформировать полноценный кокон, в контроле составила 41%, а в варианте с N. bombycis - 16%) (Issi & Maslennikova, 1966; Larsson, 1979). Вылет имаго и количество прожитых дней совпадало с контролем. Микроспоридий можно было найти в 100% случае во всех насекомых в околоплодных тканях, трахеях и даже в яйцах паразитоида, что говорит о возможности передачи нетипичной микроспоридии посредством введения инфицированных яиц. Кроме того, есть вероятность надрыва тканей около яиц и передачи микроспоридий вместе с яйцом через инфицированный яйцеклад. Эти наблюдения важны для совершенствования подходов к борьбе с вредными чешуекрылыми насекомыми.