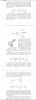Тема: СИНТЕЗ И РЕАКЦИОННАЯ СПОСОБНОСТЬ 4-АРИЛ- И 4-АРИЛ-3-КАРБЭТОКСИ-6-ТРИФТОРМЕТИЛ-2-ПИРОНОВ
Характеристики работы
Закажите новую по вашим требованиям
Представленный материал является образцом учебного исследования, примером структуры и содержания учебного исследования по заявленной теме. Размещён исключительно в информационных и ознакомительных целях.
Workspay.ru оказывает информационные услуги по сбору, обработке и структурированию материалов в соответствии с требованиями заказчика.
Размещение материала не означает публикацию произведения впервые и не предполагает передачу исключительных авторских прав третьим лицам.
Материал не предназначен для дословной сдачи в образовательные организации и требует самостоятельной переработки с соблюдением законодательства Российской Федерации об авторском праве и принципов академической добросовестности.
Авторские права на исходные материалы принадлежат их законным правообладателям. В случае возникновения вопросов, связанных с размещённым материалом, просим направить обращение через форму обратной связи.
📋 Содержание
Практическая значимость работы 4
Положения, выносимые на защиту 4
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ 5
ЗАКЛЮЧЕНИЕ 25
Список литературы 26
📖 Введение
2//-11иран-2-оны и их аннелированные аналоги широко распространены в природе. Этот гетероциклический фрагмент, являясь по сути поликетидом, входит в структуру многих биологически активных соединений, выделенных из растений, животных, насекомых, морских организмов, бактерий и грибов. Природные производные 2-пирона выполняют защитные функции, являются биосинтетическими интермедиатами или метаболитами и тем самым представляют важный для фармацевтической химии объект исследования. Химия 2-пиронов очень богата, поскольку их структура содержит три электрофильных центра (атомы С-2, С-4 и С-6) в составе двух фрагментов (сопряженного диена и лактона). Кроме того, при взаимодействии с нуклеофилами имеется возможность раскрытия пиронового кольца с уходом карбоксилата или енолята и последующей рециклизации в карбо- и гетероциклы.
Введение трифторметильной группы в пироновую систему имеет двойной положительный эффект. С одной стороны, ее электроноакцепторный характер повышает электрофильность субстрата, делая его более активным в реакциях с нуклеофилами по сравнению с нефторированным аналогом, а с другой стороны, целый ряд специфических особенностей СРз-группы, таких как усиление связывающих свойств, метаболическая стабильность и липофильность, позволяют рассматривать ее в качестве фармакофорного заместителя и рассчитывать на положительный эффект при поиске биоактивных молекул.
Однако, в литературе описано совсем немного методов получения трифторметилированных 2-пиронов, а исследования их химических свойств в основном ограничиваются типичными для а-пиронов реакциями, такими как участие в роли диена в реакциях циклоприсоединения и образование пиридонов под действием первичных аминов. В свете этого, разработка новых и эффективных способов синтеза фторалкилированных 2-пиронов из простых и доступных прекурсоров, а также изучение их реакционной способности, представляет актуальную задачу.
В качестве объекта исследования наше внимание привлекли ранее неописанные 4-арил-6-трифторметил-2-пироны, в структуре которых присутствует как активированный СРз-группой электрофильный центр, так и фрагмент коричной кислоты, широко распространенный в природных соединениях. Учитывая тот факт, что в живых организмах пироны встречаются зачастую в виде конденсированных систем, отдельное внимание было уделено методам аннелирования исследуемых соединений карбо- и гетероциклами.
Целью диссертационной работы была разработка эффективного метода синтеза замещенных 6-трифторметил-2.Н-пиран-2-онов и исследование особенностей их химических свойств, обусловленных структурой и наличием трифторметильной группы, исходя из чего были сформулированы следующие задачи:
- синтез 4-арил-3-карбэтокси-6-трифторметил-2.Н-пиран-2-онов и 4-арил-6- трифторметил-2.Н-пиран-2-онов;
• изучение взаимодействия полученных соединений с O-, S-, N- и
С-нуклеофилами;
• изучение реакции циклоприсоединения с азометин-илидом;
• получение на основе исследуемых соединений [Даннелированных
производных 2-пирона.
Научная новизна и теоретическая значимость работы:
Получены новые представители ряда 6-трифторметил-2-пиронов: 4-арил-6- трифторметил-2#-пиран-2-оны и этил-4-арил-2-оксо-6-трифторметил-2#-пиран-3- карбоксилаты.
Исследованы реакции 4-арил-6-трифторметил-2#-пиран-2-онов с гидроксидом и гидросульфидом натрия, первичными аминами, гидразинами и гидроксиламином, которые сопровождались замещением гетероатома в цикле. В реакциях с аминами показана предпочтительность начальной атаки нуклеофила по атому С-6 и промежуточное образование соответствующих 6-гидрокси-5,6-дигидропиридонов, предложен механизм реакции.
Впервые осуществлена реакция [3+2]-циклоприсоединения 2-пиронов с У-метилазометин-илидом, которая протекает по связи С5-С6 без раскрытия пиранового цикла и дает 2,4а,5,6,7,7а-гексагидропирано[2,3-с]пиррол-2-оны.
Впервые осуществлена реакция 2-пиронов с азидом натрия, приводящая в результате раскрытия цикла и рециклизации к (Т)-3-(5-трифторметил-1,2,3-триазол-4- ил)коричным кислотам. Для 3-карбэтоксипиронов подобраны условия селективного образования индивидуальных геометрических изомеров продуктов.
Показано, что этил-4-арил-2-оксо-6-трифторметил-2Я-пиран-3-карбоксилаты под действием концентрированной серной кислоты циклизуются в ранее неизвестные индено[2,1-с]пиран-1,9-дионы, которые в условиях реакции Шмидта превращаются в пирано[3,4-с]хинолин-4,5-дионы...
✅ Заключение
2. Взаимодействие 4-арил-6-трифторметил-2.Н-пиран-2-онов с гидроксидом натрия, гидразином и гидроксиламином сопровождается образованием 6-гидрокси-5,6- дигидро-2-пиронов и 6-гидрокси-5,6-дигидро-2-пиридонов.
3. Реакции 6-трифторметил-2-пиронов, 4-пиронов и их конденсированных
производных с азидом натрия приводят к трифторметил-1,2,3-триазолам. В случае 4-арил-3 -карбэтокси-6-трифторметил-2Я-пиран-2-онов, варьируя растворитель,
могут быть получены индивидуальные геометрические изомеры соответствующих моноэтиловых эфиров диарилметиленмалоновых кислот.
4. Нестабилизированный А-метилазометин-илид вступает в реакцию [3+2]-
циклоприсоединения с 2-пиронами, активированными электроноакцепторными заместителями, по связи С5-С6 с образованием пирано[2,3-с]пирролидинов. Донорные и объемные группы резко ухудшают выход продукта.
5. Взаимодействие 4-арил-3-карбэтокси-6-трифторметил-2А-пиран-2-онов с
А-метилазометин-илидом частично сопровождается нуклеофильной атакой по положению 4 пиронового цикла, приводящей в конечном счете к образованию 2-трифторметилпирролов.
6. Этил-4-арил-2-оксо-6-трифторметил-2А-пиран-3-карбоксилаты при внутри
молекулярном ацилировании по Фриделю-Крафтсу превращаются в индено[2,1- с]пиран-1,9-дионы, способные в условиях реакции Шмидта трансформироваться в пирано[3,4-с]хинолин-4,5-дионы.
Перспективы дальнейшей разработки темы исследования.
В результате проделанной работы были получены многочисленные производные коричной кислоты, интересные с точки зрения биологической активности как сами по себе, так и в плане получения на их основе других соединений, содержащих важные фармакофорные фрагменты, в первую очередь индановый, тетралиновый, хинолиновый, изохинолиновый. Найденное новое взаимодействие
фторалкилированных 2- и 4-пиронов с азидом натрия позволяет получать широкий круг функционализированных 1,2,3-триазолов.